Le cancer est une maladie complexe, souvent causée par de petits changements dans les mécanismes de nos cellules. Un acteur clé fréquemment impliqué est une protéine appelée BRAF. Aujourd’hui, une nouvelle recherche passionnante met en lumière comment les formes mutées de BRAF provoquent le cancer et, surtout, révèle une façon novatrice de potentiellement les arrêter. Cette étude, menée par une équipe de l’IRIC de l’Université de Montréal, publiée dans Science, offre un nouvel espoir pour le développement de traitements anticancéreux plus efficaces.
Contenu
Voici l’essentiel :
- Environ la moitié des cancers impliquent des problèmes avec un système de communication cellulaire appelé voie MAPK.
- BRAF agit comme un interrupteur ‘marche/arrêt’ central dans ce système, normalement strictement contrôlé.
- Les mutations de BRAF peuvent le bloquer en position ‘marche’, entraînant une croissance cellulaire incontrôlée.
- Les chercheurs ont découvert que BRAF muté y parvient en changeant sa forme pour imiter sa forme active, dupant essentiellement la cellule.
- Mieux encore : ils ont trouvé de petites molécules capables de forcer ce BRAF muté et récalcitrant à retrouver sa forme correcte, ‘inactivée’.
Le problème BRAF : Un interrupteur moléculaire qui se dérègle
Imaginez que vos cellules disposent d’un système téléphonique interne sophistiqué (la voie MAPK) qui les aide à répondre aux signaux du monde extérieur. BRAF est un opérateur critique dans ce système, agissant comme un interrupteur qui ne doit être activé ‘marche’ que lorsque cela est nécessaire. Normalement, BRAF possède des contrôles intégrés qui le maintiennent dans un état ‘inactif’ – considérez cela comme un verrou de sécurité appelé « auto-inhibition ».
Cependant, certaines erreurs génétiques, connues sous le nom de mutations oncogéniques, peuvent affecter la protéine BRAF. Ces mutations sont couramment trouvées dans divers cancers, notamment le mélanome (cancer de la peau), les cancers de la thyroïde, du côlon et du poumon. Lorsque BRAF est muté, il peut contourner son verrou de sécurité normal et devenir constamment ‘marche’, ce qui amène la cellule à recevoir des signaux de croissance non-stop. Cette croissance incontrôlée est une caractéristique du cancer.
Pendant longtemps, les scientifiques savaient que ces mutations causaient le problème, mais précisément comment la protéine BRAF altérée parvenait à échapper au contrôle n’était pas entièrement compris.
Percer le secret : Une nouvelle forme trompeuse
Utilisant des techniques d’imagerie avancées, en particulier la microscopie cryo-électronique (qui permet aux scientifiques de voir la structure 3D détaillée de minuscules protéines), l’équipe de l’Université de Montréal, dirigée par le professeur Marc Therrien, a scruté le monde de BRAF muté.
Ce qu’ils ont découvert était fascinant : les formes mutées de BRAF ne se contentent pas de casser le verrou de sécurité ; elles adoptent une forme structurelle qui semble presque identique à l’état naturellement actif de BRAF. C’est comme si la protéine mutée mettait un déguisement parfait, trompant les points de contrôle internes de la cellule en leur faisant croire qu’elle est censée être active. Cela permet au BRAF récalcitrant de déclencher des voies de signalisation sans restriction, entraînant une prolifération cellulaire illimitée.
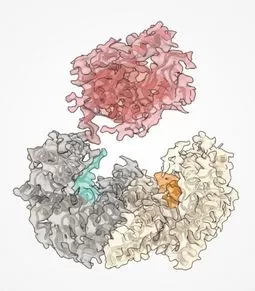 Représentation de la structure de la protéine BRAF en couleur saumon. D'autres protéines (chaperonnes) sont montrées l'aidant à se replier.
Représentation de la structure de la protéine BRAF en couleur saumon. D'autres protéines (chaperonnes) sont montrées l'aidant à se replier.
Ils ont identifié un segment spécifique de la protéine appelé hélice alpha-C. Dans le BRAF sain, cette hélice est positionnée de manière à aider à maintenir la protéine inactive. Mais dans les formes mutées et cancérigènes, cette hélice alpha-C déplace sa position pour correspondre à l’endroit où elle se trouverait dans une protéine normalement active. Ce changement structurel subtil est la clé de son comportement trompeur.
Une solution potentielle : Forcer l’interrupteur à revenir à ‘inactif’
Comprendre comment BRAF muté échappe au contrôle est une étape majeure, mais la recherche ne s’est pas arrêtée là. L’équipe a ensuite exploré la possibilité d’utiliser de petites molécules similaires à des médicaments pour cibler cette hélice alpha-C cruciale et influencer sa position.
Dans une percée significative, certaines des molécules qu’ils ont testées ont pu interagir avec la protéine BRAF mutée d’une manière qui a forcé l’hélice alpha-C à revenir à sa position ‘inactive’. Cela a effectivement ramené la forme hyperactive de BRAF, favorisant le cancer, à son état normal, inactif et auto-inhibé.
C’est une découverte puissante. La plupart des médicaments ciblant BRAF agissent actuellement en bloquant le signal en aval après que BRAF soit déjà actif. Cette nouvelle approche suggère qu’il pourrait être possible d’aborder le problème plus tôt en forçant la protéine mutée elle-même à retrouver une forme inoffensive avant même qu’elle ne puisse commencer à signaler.
La capacité de changer complètement la forme d’une protéine mutée à l’aide d’une molécule thérapeutique est une première dans ce domaine spécifique de recherche et ouvre des possibilités passionnantes.
Ce que cela signifie pour les futurs traitements anticancéreux
Cette étude fournit des informations cruciales sur les mécanismes fondamentaux de la manière dont les mutations BRAF contribuent au cancer. En comprenant les changements structurels spécifiques et le rôle de l’hélice alpha-C, les scientifiques peuvent désormais travailler à concevoir et à optimiser des classes de médicaments entièrement nouvelles.
Au lieu de simplement bloquer les effets du BRAF déréglé, de futures thérapies pourraient potentiellement être développées pour cibler spécifiquement et ‘reconvertir’ ces protéines mutées, les forçant à retrouver un état inactif. Cela pourrait être une manière plus précise et efficace de neutraliser les cancers liés à BRAF muté. Bien que cette recherche soit une étape fondamentale et que plus de travail soit nécessaire, elle ouvre une nouvelle voie prometteuse pour la découverte de médicaments et offre de l’espoir pour de meilleurs traitements pour les patients touchés par les cancers porteurs de la mutation BRAF.
Pour en savoir plus sur la recherche sur le cancer et les sujets connexes, explorez ces ressources : [Link to relevant research section 1], [Link to relevant research section 2].
